20 Exemplos De Fenômenos Físicos E Químicos | 2024: Mergulhe no fascinante mundo da física e da química explorando 20 exemplos práticos que demonstram a diferença entre transformações físicas e químicas da matéria. Descobriremos como essas transformações impactam nosso dia a dia, desde a simples ebulição da água até processos complexos como a fotossíntese. Prepare-se para uma jornada de descobertas que revelará a beleza e a complexidade dos fenômenos que nos cercam.
Este guia abrangente apresenta exemplos claros e concisos, facilitando a compreensão dos conceitos fundamentais. Através de descrições detalhadas e exemplos do cotidiano, você aprenderá a identificar e diferenciar fenômenos físicos, onde a composição da matéria permanece inalterada, de fenômenos químicos, que resultam em novas substâncias. Acompanhe-nos nessa exploração e amplie seu conhecimento sobre o mundo físico e químico que nos rodeia.
Classificação dos Fenômenos
A compreensão da diferença entre fenômenos físicos e químicos é fundamental para o estudo da ciência. Ambos envolvem mudanças na matéria, mas essas mudanças diferem significativamente em sua natureza e na composição da matéria envolvida. Fenômenos físicos alteram a forma ou estado físico da matéria, mas não sua composição química, enquanto fenômenos químicos resultam em mudanças na composição química da matéria, formando novas substâncias.
Em essência, a distinção reside na formação ou quebra de ligações químicas. Fenômenos físicos são reversíveis em muitos casos, enquanto fenômenos químicos geralmente não são. A seguir, exploraremos essa distinção com exemplos concretos.
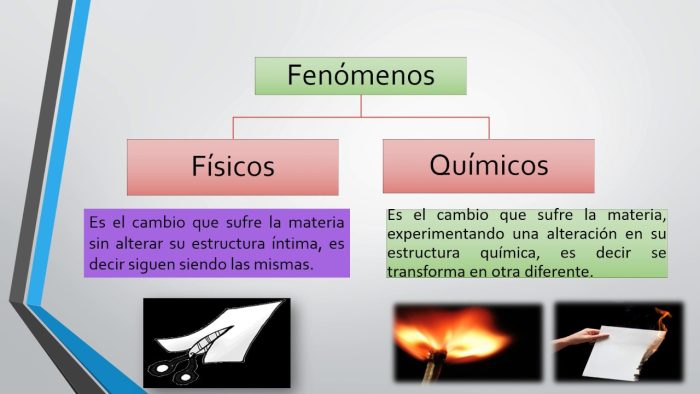
Diferença entre Fenômenos Físicos e Químicos
Fenômenos físicos envolvem mudanças no estado físico da matéria, como mudanças de fase (sólido, líquido, gasoso), tamanho, forma ou estado de agregação, sem alterar a composição química da substância. Exemplos incluem a fusão do gelo (água sólida para água líquida), a evaporação da água (água líquida para vapor de água) e a dissolução do açúcar em água (o açúcar permanece quimicamente inalterado).
Já os fenômenos químicos envolvem a transformação de uma ou mais substâncias em outras substâncias diferentes, com mudanças na composição química. Isso acontece através da formação ou quebra de ligações químicas, resultando em novas substâncias com propriedades diferentes. Exemplos incluem a combustão da madeira (produzindo cinzas e gases), a ferrugem do ferro (oxidação do ferro) e a digestão dos alimentos (reações químicas complexas que quebram moléculas grandes em menores).
Exemplos de Fenômenos Físicos e Químicos

A tabela abaixo apresenta 20 exemplos de fenômenos físicos e químicos, categorizados e brevemente descritos.
| Fenômeno | Tipo | Descrição | Observação |
|---|---|---|---|
| Fusão do gelo | Físico | Mudança de estado físico de sólido para líquido. | Reversível |
| Evaporação da água | Físico | Mudança de estado físico de líquido para gasoso. | Reversível (condensação) |
| Dissolução do sal em água | Físico | O sal se dissolve na água, mas mantém sua composição química. | Reversível (evaporação da água) |
| Quebra de um copo de vidro | Físico | Alteração na forma física, sem alteração na composição química. | Irreversível (na prática) |
| Dobrar um pedaço de papel | Físico | Mudança na forma física, sem alteração na composição química. | Reversível (parcialmente) |
| Combustão da madeira | Químico | Reação química que produz cinzas, gases e calor. | Irreversível |
| Ferrugem do ferro | Químico | Oxidação do ferro, formando óxido de ferro. | Irreversível |
| Digestão dos alimentos | Químico | Reações químicas complexas que quebram moléculas grandes em menores. | Irreversível |
| Fotossíntese | Químico | Plantas convertem dióxido de carbono e água em glicose e oxigênio. | Irreversível (na planta) |
| Queima de um fósforo | Químico | Reação de combustão que produz luz e calor. | Irreversível |
| Ebulição da água | Físico | Mudança de estado físico de líquido para gasoso a uma temperatura específica. | Reversível (condensação) |
| Sublimação do gelo seco | Físico | Mudança de estado físico de sólido para gasoso diretamente. | Reversível (deposição) |
| Mistura de água e álcool | Físico | Formação de uma mistura homogênea, sem reação química. | Reversível (destilação) |
| Cozimento de um ovo | Químico | Desnaturação das proteínas do ovo pelo calor. | Irreversível |
| Queima de gás natural | Químico | Reação de combustão que produz calor e dióxido de carbono. | Irreversível |
| Respiração celular | Químico | Reações químicas que liberam energia a partir da glicose. | Irreversível |
| Formação de chuva | Físico | Condensação do vapor de água na atmosfera. | Reversível (evaporação) |
| Dissolução do açúcar em água | Físico | O açúcar se dissolve na água, sem alterar sua composição química. | Reversível (evaporação da água) |
| Queima de papel | Químico | Reação de combustão que produz cinzas e gases. | Irreversível |
| Corrosão de um metal | Químico | Reação química entre o metal e o ambiente, causando deterioração. | Irreversível |
Comparação de Fenômenos Físicos e Químicos
A comparação a seguir destaca as diferenças na composição da matéria entre cinco fenômenos físicos e cinco fenômenos químicos.
Fenômenos Físicos:
- Fusão do gelo: A água muda de estado físico, mas continua sendo H₂O.
- Evaporação da água: A água muda de líquido para gás, mas sua composição molecular permanece inalterada (H₂O).
- Dissolução do açúcar em água: O açúcar se dispersa na água, mas suas moléculas permanecem intactas (sacarose).
- Quebra de um copo de vidro: O vidro se fragmenta, mas sua composição química (sílica) não se altera.
- Mistura de areia e água: A areia e a água se misturam, mas não reagem quimicamente, mantendo suas composições individuais.
Fenômenos Químicos:
- Combustão da madeira: A madeira (celulose) reage com o oxigênio, formando dióxido de carbono, água e cinzas, alterando completamente sua composição.
- Ferrugem do ferro: O ferro reage com o oxigênio e a água, formando óxido de ferro (ferrugem), uma substância com composição química diferente do ferro.
- Digestão dos alimentos: Moléculas complexas de alimentos são quebradas em moléculas menores, alterando sua composição química para facilitar a absorção pelo organismo.
- Queima de um fósforo: A cabeça do fósforo sofre uma reação de combustão, produzindo novas substâncias com composição química diferente dos materiais originais.
- Fotossíntese: Dióxido de carbono e água são transformados em glicose e oxigênio, uma mudança significativa na composição química.
Exemplos Detalhes de Fenômenos Físicos e Químicos: 20 Exemplos De Fenômenos Físicos E Químicos | 2024
Este texto detalha exemplos específicos de fenômenos físicos e químicos, explorando as transformações da matéria e energia envolvidas em cada processo. A compreensão desses processos é fundamental para a compreensão da ciência em geral. A distinção entre fenômenos físicos e químicos reside na alteração da composição da matéria. Fenômenos físicos envolvem mudanças de estado, forma ou tamanho, sem alterar a composição química da substância.
Já os fenômenos químicos resultam em novas substâncias com propriedades diferentes das substâncias iniciais.
Ebulição da Água: Um Fenômeno Físico

A ebulição da água é um exemplo clássico de fenômeno físico. Quando a água é aquecida, a energia térmica aumenta a energia cinética das moléculas de H₂O. À medida que a temperatura se aproxima dos 100°C (ao nível do mar), a energia cinética supera as forças intermoleculares que mantêm as moléculas unidas no estado líquido. As moléculas escapam da superfície do líquido na forma de vapor, um processo chamado vaporização.
Durante a ebulição, a temperatura permanece constante (100°C ao nível do mar) enquanto toda a energia fornecida é usada para a mudança de fase, de líquido para gás. Não há alteração na composição química da água; ela continua sendo H₂O, apenas em um estado físico diferente. A imagem mostraria uma panela com água fervendo, bolhas subindo à superfície e vapor sendo liberado.
A imagem descreveria visualmente a transição do estado líquido para o gasoso, mantendo a composição molecular da água inalterada.
Combustão da Madeira: Um Fenômeno Químico
A combustão de um pedaço de madeira é um exemplo complexo de fenômeno químico, envolvendo uma reação de oxidação exotérmica. A madeira é composta principalmente de celulose, lignina e outras substâncias orgânicas. Na presença de calor e oxigênio (O₂), essas substâncias reagem quimicamente, quebrando suas ligações químicas e formando novas substâncias, como dióxido de carbono (CO₂), água (H₂O) e cinzas.
Esse processo libera energia na forma de calor e luz. A transformação química é evidente pela mudança na composição da madeira: ela se transforma em cinzas, CO₂, H₂O e outros produtos da combustão. A imagem ilustraria um pedaço de madeira queimando, mostrando as chamas, a fumaça e as cinzas resultantes. A descrição detalharia a transformação da madeira em novas substâncias, como CO2 e H2O, e a liberação de energia na forma de calor e luz.
A imagem mostraria claramente a mudança na composição da matéria.
Tabela de Fenômenos Físicos e Químicos

A tabela abaixo lista 10 exemplos de fenômenos físicos e 10 exemplos de fenômenos químicos, com descrições detalhadas das imagens correspondentes.
| Fenômeno | Descrição |
|---|---|
| Derretimento do gelo | Imagem de um cubo de gelo derretendo, mostrando a mudança de estado físico de sólido para líquido. Observa-se a transformação gradual do gelo sólido em água líquida, sem alteração na composição química (H₂O). |
| Evaporação da água | Imagem de um copo d’água em um ambiente quente, mostrando a diminuição gradual do nível da água devido à transformação em vapor. A água líquida passa para o estado gasoso, sem mudança na composição molecular. |
| Dissolução do sal na água | Imagem de cristais de sal se dissolvendo em um copo d’água, mostrando a dispersão dos íons de sódio e cloro na água. Embora haja uma mudança de estado físico, a composição química do sal e da água permanece inalterada. |
| Quebra de um copo de vidro | Imagem de um copo de vidro quebrado em vários pedaços, mostrando a fragmentação do material, mas sem alteração na composição química do vidro. |
| Dobramento de um pedaço de papel | Imagem de um pedaço de papel sendo dobrado, mostrando a mudança na forma do papel, sem alteração na sua composição química. |
| Queima de papel | Imagem de um pedaço de papel queimando, mostrando a transformação do papel em cinzas, fumaça e gases. A composição química do papel muda completamente, formando novas substâncias. |
| Ferrugem em um prego | Imagem de um prego enferrujado, mostrando a formação de óxido de ferro (ferrugem) na superfície do prego. O ferro reage com o oxigênio do ar, formando uma nova substância com propriedades diferentes. |
| Digestão de alimentos | Imagem representando o processo digestivo, mostrando a quebra de moléculas complexas de alimentos em moléculas menores através de reações químicas. A composição química dos alimentos é alterada durante a digestão. |
| Fotossíntese | Imagem de uma planta realizando fotossíntese, mostrando a conversão de dióxido de carbono e água em glicose e oxigênio, com a energia solar como catalisador. Uma clara transformação química ocorre, com a formação de novas moléculas orgânicas. |
| Cozimento de um bolo | Imagem de um bolo assando no forno, mostrando as mudanças químicas e físicas que ocorrem na massa durante o cozimento. As proteínas e açúcares da massa sofrem transformações químicas, resultando em uma textura e sabor diferentes. |
| Congelamento da água | Imagem da água passando do estado líquido para o sólido (gelo), mostrando a mudança de estado físico sem alteração na composição química (H₂O). |
| Sublimação do gelo seco | Imagem do gelo seco sublimando, passando diretamente do estado sólido para o gasoso (CO2), sem passar pelo estado líquido. A composição química permanece inalterada. |
| Queima de álcool | Imagem do álcool queimando, mostrando a reação química entre o álcool e o oxigênio, formando dióxido de carbono e água. A composição química do álcool muda completamente. |
| Reação de neutralização | Imagem de uma reação ácido-base, mostrando a reação entre um ácido e uma base, formando sal e água. Uma nova substância é formada, com propriedades diferentes das substâncias iniciais. |
| Eletrólise da água | Imagem da eletrólise da água, mostrando a decomposição da água em hidrogênio e oxigênio por meio de corrente elétrica. A composição química da água é alterada, formando novas substâncias. |
| Respiração celular | Imagem representando a respiração celular, mostrando a quebra de glicose em dióxido de carbono e água, liberando energia. A composição química da glicose muda completamente. |
| Corrosão do metal | Imagem de um metal corroído, mostrando a reação química entre o metal e o ambiente, formando compostos metálicos. A composição química do metal é alterada. |
| Queima de gás natural | Imagem do gás natural queimando, mostrando a reação química entre o gás natural (principalmente metano) e o oxigênio, formando dióxido de carbono e água. A composição química do gás natural muda completamente. |
| Fotodegradação do plástico | Imagem de um plástico exposto ao sol, mostrando a degradação do plástico devido à ação da luz solar. A composição química do plástico é alterada. |
| Formação da chuva ácida | Imagem representando a formação da chuva ácida, mostrando a reação dos óxidos de enxofre e nitrogênio com a água na atmosfera, formando ácidos. Novas substâncias são formadas com propriedades diferentes das iniciais. |
Aplicações e Implicações dos Fenômenos
A compreensão e aplicação dos fenômenos físicos e químicos são cruciais para o desenvolvimento tecnológico e a resolução de problemas em diversas áreas, desde a construção civil até a produção de alimentos. A capacidade de prever e controlar esses fenômenos permite inovações e melhorias significativas em nossa vida diária. A seguir, exploraremos algumas aplicações e implicações relevantes.
Implicações da Oxidação do Ferro na Construção Civil

A oxidação do ferro, popularmente conhecida como ferrugem, é um processo químico que resulta na corrosão do metal. Na construção civil, isso representa um sério problema, pois compromete a estrutura e a durabilidade das edificações. A ferrugem causa a fragilização do aço, elemento estrutural fundamental em prédios, pontes e outras construções. Para minimizar os efeitos da oxidação, são utilizados diversos métodos, como a galvanização (revestimento com zinco), a pintura com tintas protetoras e o uso de aço inoxidável, que possui maior resistência à corrosão.
A falta de prevenção adequada à oxidação pode levar a acidentes graves, comprometendo a segurança e a estabilidade das estruturas. O custo da manutenção e reparação de estruturas danificadas pela corrosão também é significativo.
Fotossíntese: Transformação Química Fundamental para a Vida na Terra
A fotossíntese é um processo químico essencial para a vida na Terra. Nesse processo, plantas e outros organismos fotossintéticos convertem energia luminosa em energia química, na forma de glicose. A equação simplificada da fotossíntese é: 6CO 2 + 6H 2O + Luz → C 6H 12O 6 + 6O 2. A glicose produzida serve como fonte de energia para o próprio organismo e para a cadeia alimentar, enquanto o oxigênio liberado é fundamental para a respiração aeróbica de animais e plantas.
Sem a fotossíntese, não haveria oxigênio na atmosfera e a vida como a conhecemos seria impossível. A compreensão da fotossíntese é crucial para o desenvolvimento de tecnologias voltadas à produção de biocombustíveis e para a pesquisa sobre a mitigação das mudanças climáticas.
Contribuições da Compreensão de Fenômenos Físicos e Químicos para o Desenvolvimento de Novas Tecnologias, 20 Exemplos De Fenômenos Físicos E Químicos | 2024

A compreensão dos fenômenos físicos e químicos é a base para o desenvolvimento de inúmeras tecnologias. Alguns exemplos incluem:
- Desenvolvimento de materiais mais resistentes e leves: A nanotecnologia, por exemplo, utiliza princípios da física e da química para criar materiais com propriedades aprimoradas, como maior resistência, leveza e flexibilidade, aplicados em diversas áreas, da construção civil à aeronáutica.
- Criação de baterias mais eficientes: A compreensão de reações químicas redox permite o desenvolvimento de baterias com maior capacidade de armazenamento de energia e maior durabilidade, essenciais para a mobilidade elétrica e o armazenamento de energia renovável.
- Avanços na medicina: A química medicinal utiliza princípios químicos para desenvolver novos fármacos e tratamentos para doenças, enquanto a física médica contribui com tecnologias de diagnóstico por imagem e radioterapia.
- Desenvolvimento de tecnologias de energia limpa: A compreensão de fenômenos físicos e químicos relacionados à energia solar, eólica e geotérmica permite o desenvolvimento de tecnologias de energia renovável mais eficientes e sustentáveis.
- Progressos na eletrônica: A miniaturização de componentes eletrônicos e o desenvolvimento de novos materiais semicondutores dependem profundamente da compreensão de fenômenos físicos e químicos a nível atômico e molecular.
Aplicações de Fenômenos Físicos e Químicos na Indústria Alimentícia
A indústria alimentícia utiliza amplamente os princípios da física e da química para garantir a qualidade, segurança e conservação dos alimentos.
| Tipo de Fenômeno | Aplicação | Indústria | Descrição |
|---|---|---|---|
| Físico (Transferência de Calor) | Pasteurização | Laticínios, bebidas | Utiliza calor para eliminar microrganismos, prolongando a vida útil do produto. |
| Físico (Congelamento) | Conservação de alimentos | Diversos | Reduz a atividade enzimática e microbiana, preservando a qualidade do alimento. |
| Físico (Pressão) | Enlatamento | Diversos | Utiliza pressão para esterilizar e conservar os alimentos em embalagens hermeticamente fechadas. |
| Físico (Desidratação) | Secagem de frutas e legumes | Diversos | Remove a água, inibindo o crescimento de microrganismos e aumentando a vida útil. |
| Físico (Filtração) | Clarificação de sucos | Bebidas | Remove partículas sólidas, melhorando a aparência e o sabor do produto. |
| Químico (Reações de Fermentação) | Produção de iogurte, queijos, pães | Laticínios, panificação | Utiliza microrganismos para transformar açúcares em ácido lático ou outros compostos, conferindo sabor e textura característicos. |
| Químico (Oxidação) | Amadurecimento de frutas | Frutas e legumes | Processos químicos que alteram a cor, sabor e textura das frutas. |
| Químico (Hidrólise) | Produção de xaropes de milho | Doces | Quebra de moléculas de amido em açúcares mais simples. |
| Químico (Reações de Maillard) | Coloração e sabor em alimentos assados | Panificação, confeitaria | Reações entre aminoácidos e açúcares, gerando compostos aromáticos e cores escuras. |
| Químico (Preservação) | Adição de conservantes | Diversos | Inibição do crescimento de microrganismos, aumentando a vida útil do alimento. |
Compreender a diferença entre fenômenos físicos e químicos é fundamental para entender o mundo ao nosso redor. De processos naturais como a fotossíntese à tecnologia moderna, a aplicação desses princípios é vasta e essencial. Esperamos que este guia com 20 exemplos tenha elucidado esses conceitos, estimulando sua curiosidade e a busca por um conhecimento mais profundo sobre a ciência que governa nossas vidas.
Explore ainda mais, questione, e continue aprendendo!

